Hépatite C : le sofosbuvir (Sovaldi) approuvé en Europe
Voilà qu’enfin s’ouvre l’ère du traitement de l’hépatite C sans interféron. Attendu par de nombreuses personnes vivant avec le VHC, le sofosbuvir (Sovaldi) a obtenu son autorisation européenne de mise sur le marché (AMM) le 17 janvier. Quel est le contenu de cette AMM ? Quand le médicament sera-t-il effectivement disponible ? Quels sont les schémas d’utilisation, leur durée, leur efficacité, leurs effets indésirables ? Et quel sera le prix de ce nouveau médicament ? Seronet vous dit tout.

Cette AMM fait suite à une évaluation accélérée par l'Agence européenne des médicaments (EMA), réservée aux nouveaux médicaments qui présentent un intérêt majeur en matière de santé publique. Elle vaut pour les 28 pays de l’Union européenne.
Un agent anti-viral direct
Le sofosbuvir est un agent anti-viral direct (AVD), c’est-à-dire qu’il agit directement sur le VHC, en bloquant une étape de son cycle de réplication. Plus précisément, il inhibe une enzyme, la polymérase (techniquement, c’est un inhibiteur nucléotidique de la polymérase du VHC). Il est commercialisé par la firme Gilead.
Sa posologie est d’un comprimé (400 mg) par jour. Soit, beaucoup plus simple que les actuels télaprévir (Incivo, 3 comprimés 2 fois par jour) et bocéprévir (Victrelis, 4 gélules 2 fois par jour).
Le sofosbuvir ne s’utilise pas seul, mais en association avec d’autres médicaments anti-VHC. Pour l’heure, il s’agit essentiellement de la ribavirine. A laquelle, mauvaise nouvelle, il faut ajouter dans certains cas, de l’interféron. Assez rapidement cependant, il devrait être possible de se passer de la ribavirine et (surtout) de l’interféron, en combinant le sofosbuvir avec un autre AVD : le siméprévir, le daclatasvir (qui sont en cours d’évaluation par les autorités de santé) ou le lédispavir (que le laboratoire va soumettre aux autorités dans les prochaines semaines).
Efficace contre tous les génotypes
L’utilisation du sofosbuvir a été étudiée pour les génotypes de 1 à 6. L’efficacité du sofosbuvir a été établie pour les génotypes 1 (personnes naïves de traitement uniquement), 2, 3 et 4, y compris les personnes en attente d’une greffe de foie ainsi que celles co-infectées par le VIH. Génotypes qui concernent la majorité des personnes vivant avec le VHC. En revanche, les données cliniques sur les génotypes 5 et 6 (plus rares) sont limitées.
Quels schémas d’utilisation ?
Même si le sofosbuvir suscite de nombreux - et légitimes - espoirs, il n’a rien de magique. Le tableau ci-dessous résume les schémas d’utilisations recommandés selon l’AMM. En fonction du génotype du VHC, la durée de traitement est de 3 ou 6 mois (précisément, 12 ou 24 semaines).
Or ce n’est que pour le génotype 2 qu’un traitement de 3 mois sans interféron est possible. Pour le génotype 3, on a le choix : soit 3 mois avec ribavirine et interféron, soit 6 mois avec la ribavirine seule (l’efficacité est similaire). Pour les autres (1, 4, 5, 6), un traitement de 3 mois n’est possible qu’en ajoutant l’interféron. Si on est inéligible ou intolérant à l’interféron, un traitement de 6 mois s’impose, mais il est moins efficace.
Ces schémas ne sont pas différents qu’on soit co-infecté par le VIH ou non.
Lorsqu’il est utilisé avant une greffe du foie, le traitement sofosbuvir + ribavirine se fait jusqu’à la transplantation hépatique.
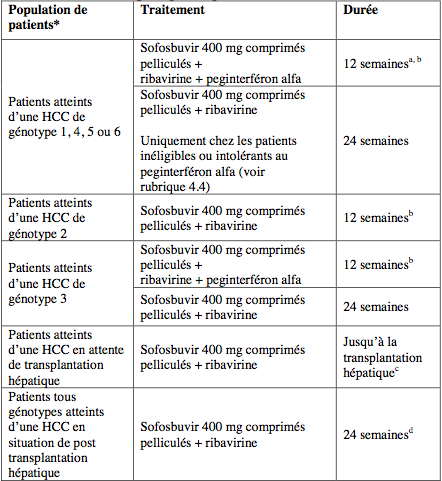
NB : dans le tableau, le sigle HCC signifie hépatite C chronique.
L’arrivée de nouveaux AVD permettra de concevoir de nouveaux schémas. Pour ne donner qu’un exemple, 3 mois de siméprévir + sofosbuvir donnent plus de 90 % d’efficacité pour le génotype 1 (sans qu’allonger la durée de traitement ou ajouter de la ribavirine ne permettent d’améliorer ce résultat).
Pas de résistances et une bonne tolérance (semble-t-il)
Le laboratoire fabriquant indique qu’environ 3 000 personnes ont reçu du sofosbuvir dans des essais de phase 2 et 3. Dans ces essais, il n’y a pas eu de résistances observées, et le sofosbuvir a été bien toléré. Cela devra être vérifié dans la vraie vie.
Dans le cadre des essais avec bithérapie interféron + ribavirine, les effets relevés chez au moins 10 % des personnes sont cohérents avec ceux qu’on connait avec la bithérapie : fatigue, maux de tête, nausées, insomnies, vertiges, prurit (démangeaisons sévères) et anémie (baisse des globules rouges).
Des retours d’utilisation des hépatologues, il ressort que l’effet principal du sofosbuvir est la fatigue, et que lorsqu’on l’utilise avec la ribavirine seule, l’anémie est moins forte qu’avec l’interféron, et nécessite moins souvent une prise en charge spécifique.
Peu d’interactions
Un des points forts du sofosbuvir est qu’il comporte peu d’interactions avec les médicaments anti-VIH, ce qui va faciliter le traitement des personnes co-infectées. Selon le résumé des caractéristiques du produit (RCP) inclus dans le protocole temporaire d’utilisation, on sait que le sofosbuvir peut notamment s’utiliser sans ajustements de dose avec :
- les médicaments immuno-suppresseurs suivants : ciclosporine (avec précaution) et tacrolimus ;
- la méthadone (traitement de substitution aux opiacés) ;
- les médicaments anti-VIH suivants : efavirenz (Sustiva), emtricitabine et ténofovir (Truvada), rilpivirine (Edurant, Eviplera), darunavir/ritonavir (Prezista/Norvir), raltégravir (Isentress).
En revanche, il ne doit pas être utilisé avec les produits à base de millepertuis, une plante parfois utilisée dans le traitement de dépressions légères à modérées et de troubles de l'humeur.
Quand sera-t-il disponible ?
Depuis plusieurs mois, Sovaldi est déjà disponible en ATU (autorisation temporaire d’utilisation) pour des personnes ne disposant pas d’alternatives thérapeutiques appropriées et répondant aux critères suivants :
- fibrose avancée ou cirrhose ;
- sur liste d’attente de greffe du foie ;
- après une greffe du foie mais avec une récurrence du VHC agressive, et espérance de vie inférieure à 12 mois sans traitement.
La disponibilité du produit après l’AMM a fait l’objet d’un combat des associations à l’automne 2013. En effet, le projet de loi de financement de la sécurité sociale, tel que préparé par le gouvernement, restreignait l’accès rapide aux médicaments innovants ayant fait l’objet d’ATU. Au final, le texte adopté par le parlement est plus souple.
Il prévoit que dans les jours qui viennent, le produit sera accessible et remboursé pour toutes les personnes entrant dans les critères de l’ATU. De plus, la Haute autorité de santé (HAS) doit déterminer au plus tard un mois après l’AMM (d’ici au 17 février 2014) quels groupes patients doivent bénéficier d’un accès immédiat au médicament et de son remboursement. Trois conditions sont prévues par la loi : 1- être sans ; 2- ou en échec, 3- ou avec contre-indication aux alternatives thérapeutiques remboursées. L’avis sera publié sur le site de la HAS et suffira pour donner accès au remboursement.
Pour les autres personnes, il faudra attendre le circuit classique de fixation du prix, qui devrait prendre environ 1 an.
Prix fous ou prix raisonnables ?
Au niveau mondial, le prix accordé aux Etats-Unis (84 000 dollars pour 12 semaines) fait beaucoup parler. D’autant plus que le coût de production est très bas (certains l’estiment entre 50 et 100 euros pour trois mois de traitement).
En France, le coût qui prévaut actuellement est celui exigé par le laboratoire dans le cadre de l’ATU. Soit 56 000 euros pour 12 semaines de traitement (666 euros par comprimé). Sachant qu’il en faut 24 dans de fréquentes situations (112 000 euros) et jusqu’à 48 semaines en pré-transplantation (soit 224 000 euros). Des sommes considérables, que Gilead justifie notamment par de potentielles économies ultérieures en termes de suivi et de gestion des effets indésirables (diminution du nombre de consultations, moindre recours aux injections d’EPO et aux transfusions).
C’est ce prix qui restera valable le temps que le prix de remboursement définitif soit négocié avec le CEPS, le comité économique des produits de santé - où les patients ne sont pas représentés, et n’ont pas aujourd’hui leur mot à dire ! Cela prend généralement un an. Le laboratoire devra reverser aux pouvoirs publics la différence entre le prix ATU et le prix de remboursement.
Il faut espérer que Gilead sera plus raisonnable dans la négociation du prix final, faute de quoi la question de la soutenabilité du traitement des personnes vivant avec le VHC se posera avec une acuité particulière.
Car rien qu’en France, 235 000 personnes vivent avec le VHC. Pour toutes les traiter, la dépense liée au seul sofosbuvir sur une durée de 3 mois (dont on a dit qu’elle sera le plus souvent insuffisante) serait (au tarif actuel) de plus de… 13 milliards d’euros !
En Europe, ce sont 9 millions de personnes qui vivent avec le VHC. Et 150 millions à l’échelle mondiale. Qu’en est-il de l’accès dans les pays à ressources limitées ou pays à revenus intermédiaires (sans parler de pays européens confrontés aux effets de la crise comme l’Espagne, le Portugal ou la Grèce ? La question reste entière.
- Connectez-vous ou Inscrivez-vous pour publier un commentaire
- 18326 lectures
- Envoyer par mail

Commentaires
Deux modes d'administration !!! avec cette combinaison !!!
Pas mal ça 12 semaines avec interféron + riba+ sofosbuvir, parce que trois mois le temps que l'emprise de l’interféron arrive,et dur à supporter
24 semaines sofosbuvir + riba, pas mal du tout, si pas d'EI ça doublera le prix en moyenne, mais bon, avec les autres médocs qui viennent s'ajouter, ça devrait évoluer encore quelques fois, en tout cas, c'est efficace sur les coinfs c'est important, sans surcharge d'effets en plus, à voir, ce que ça va donner.
Pascal ... .. .
prix fous ou prix raisonnables ?
la santé n'a pas de prix